BORIS GROISMAN, MARÍA PAZ BIDONDO, SANTIAGO DUARTE, AGOSTINA TARDIVO,
PABLO BARBERO, ROSA LIASCOVICH
Red Nacional de Anomalías Congénitas de Argentina (RENAC), Centro Nacional de Genética Médica, Administración Nacional de Laboratorios e Institutos de Salud (A.N.L.I.S.), Ministerio de Salud de la Nación, Buenos Aires, Argentina
Resumen El objetivo del trabajo es presentar las frecuencias de anomalías congénitas (AC) estructurales mayores obtenidas por la Red Nacional de Anomalías Congénitas de Argentina (RENAC) correspondientes al año 2016, como parte de sus actividades de vigilancia de salud pública de AC. La RENAC es un sistema de vigilancia de AC oficial, nacional y de base hospitalaria. La definición de caso corresponde a recién nacidos con AC estructurales mayores, externas o internas, identificadas desde el nacimiento hasta el alta del hospital y detectadas en el examen físico, estudios complementarios, intervenciones o autopsia. Se incluyeron todos los recién nacidos vivos y los fetos muertos de 500 gramos o más. La prevalencia de AC al nacimiento se calculó como el cociente entre el número de recién nacidos vivos y fetos muertos con AC, y el número total de recién nacidos vivos y fetos muertos, en un período determinado. Según su presentación los casos con AC específicas fueron clasificados en aislados, múltiples y síndromes. La prevalencia al nacimiento de AC estructurales mayores fue de 1.59% (Intervalo de confianza del 95%: 1.55-1.64). Las anomalías específicas más frecuentes fueron: fisuras labiopalatinas, gastrosquisis, hidrocefalia, talipes equinovarus, espina bífida, polidactilia postaxial, malformación anorrectal, hernia diafragmática, quistes renales y atresia de esófago. El síndrome más frecuente fue Down. Se estimaron los casos anuales esperados y la prevalencia de AC específicas seleccionadas. En general, los datos de RENAC están dentro de los valores informados en la literatura.
Palabras clave: Argentina, prevalencia de anomalías congénitas, vigilancia de la salud pública
Abstract Descriptive epidemiology of major structural congenital anomalies in Argentina. The objective of the study is to present the frequency of congenital anomalies (CA) reported to the National Network of Congenital Anomalies of Argentina (RENAC) in the year 2016, as part of its monitoring activities. RENAC is an official, national and hospital-based surveillance system of CA. The case definition includes newborns with major structural CA, external or internal, identified from birth until hospital discharge and detected by physical examination, complementary studies, interventions or autopsy. All live newborns and stillbirths of 500 grams or more were included. The prevalence of CA at birth was calculated as the quotient between the number of live newborns and stillbirths with CA, and the total number of live newborns and stillbirths, for a given period. According to their presentation, the cases with specific CA were classified into isolated, multiple and syndromes. The prevalence at birth of major structural CA was 1.59% (95% confidence intervals 1.55-1.64). The most frequent specific anomalies were: cleft lip and palate, gastroschisis, hydrocephalus, talipes equinovarus, spina bifida, postaxial polydactyly, anorectal malformation, diaphragmatic hernia, renal cysts and esophageal atresia. The most frequent syndrome was Down´s. The expected annual cases and the prevalence of selected specific CA were estimated. RENAC data are within values reported in the literature.
Key words: Argentina, prevalence of congenital anomalies, public health surveillance
Recibido: 12-VI-2018 Aceptado: 17-VII-2018
Dirección postal: Boris Groisman, RENAC, Avenida Las Heras 2670 Piso 3, 1425 Buenos Aires, Argentina
e-mail: bgroisman@gmail.com
En las últimas décadas la mortalidad infantil ha descendido en gran parte de los países del mundo. El componente de la mortalidad infantil que más se ha reducido es el correspondiente al período postneonatal (de los 28 a los 365 días de vida), gracias al control de las enfermedades inmunoprevenibles y la desnutrición. Si bien hay heterogeneidad entre los países, el componente neonatal de la mortalidad infantil ha sido más difícil de reducir y además de la prematurez y el bajo peso, las anomalías congénitas pasaron a tener un mayor peso relativo1. En el año 2016, Argentina notificó 7093 defunciones de menores de 1 año, con una tasa de mortalidad infantil de 9.7 cada 1000 nacidos vivos2. Las defunciones infantiles debidas a anomalías congénitas en ese período fueron 1919 y explicaron más del 27% de las defunciones infantiles totales.
Las anomalías congénitas estructurales suelen ocasionar discapacidad a largo plazo. Pueden ser el resultado de uno o más factores genéticos, infecciosos, nutricionales o ambientales, o sus causas pueden ser desconocidas. La mayor parte de las anomalías congénitas se pueden prevenir3. La vacunación anti-rubeólica, el consumo adecuado de ácido fólico a través del enriquecimiento de los alimentos básicos y la atención pre-concepcional adecuada, son solo tres ejemplos de intervenciones de prevención4.
En 2010, la 63a Asamblea Mundial de la Organización Mundial de la Salud adoptó una Resolución sobre las anomalías congénitas. Entre sus propuestas, alienta a los países a desarrollar iniciativas para su prevención y les sugiere iniciar o profundizar la organización de sistemas de vigilancia5.
La Red Nacional de Anomalías Congénitas de Argentina (RENAC) es un sistema de vigilancia de anomalías congénitas estructurales mayores6. Las anomalías congénitas estructurales mayores son alteraciones de la morfología de órganos o partes del cuerpo, con impacto médico o social significativo7. En forma continua y sistemática, la RENAC realiza la recolección, análisis y diseminación de datos de salud necesarios para la planificación, implementación y evaluación de prácticas de salud pública.
Los objetivos de este trabajo son presentar los resultados obtenidos por la RENAC correspondientes al año 2016, como parte de sus actividades de vigilancia de la salud pública de anomalías congénitas y comparar los resultados con lo informado previamente en la literatura.
Materiales y métodos
La RENAC es un sistema de base hospitalaria y de alcance nacional. Los datos para el presente trabajo provienen de 160 maternidades de las 24 jurisdicciones del país: 133 son hospitales pertenecientes al subsector público y 27 son maternidades del subsector privado y/o obras sociales que formaron parte de la red en 2016. En 2016 la RENAC cubrió 305 452 nacimientos, lo cual representa una cobertura de aproximadamente 40% de los nacimientos del país. La cobertura es más elevada en el subsector público, alcanzando aproximadamente el 59%.
La definición de caso corresponde a los recién nacidos con anomalías congénitas estructurales mayores, externas o internas, identificadas desde el nacimiento hasta el alta del hospital y detectadas en el examen físico o por estudios complementarios, intervenciones o autopsia. Se incluyen todos los recién nacidos vivos, y los fetos muertos de 500 gramos o más; se excluyen aquellos que solo presentan anomalías congénitas (AC) menores y/o funcionales (mamelón pre-auricular, hipoacusia, por ejemplo).
En cada hospital participante uno o dos médicos responsables de la RENAC son los encargados de supervisar la recolección y envío de datos. Una vez recolectados los datos de cada mes, estos son enviados a la Coordinación de la RENAC. En cuanto a la información sobre las anomalías congénitas, los médicos participantes envían una descripción detallada de las mismas en un campo abierto, pudiendo incluir fotografías –previa firma del consentimiento informado– y resultados de estudios complementarios (i.e. cariotipo, imágenes).
La revisión de la descripción, la clasificación de los casos y la codificación de las anomalías congénitas es realizada por médicos genetistas de la Coordinación y se utiliza la Clasificación Internacional de Enfermedades, Décima Revisión (CIE-10) correspondiente al capítulo XVII (códigos Q00.0 a Q99.9), con la adaptación del Royal College of Pediatrics and Child Health8.
La prevalencia de anomalías congénitas al nacimiento se define como la proporción entre el número de recién nacidos vivos y fetos muertos con anomalías congénitas, y el número total de recién nacidos vivos y fetos muertos dentro de un período determinado9. Las prevalencias fueron calculadas según la distribución de Poisson, con un intervalo de confianza del 95%. Teniendo en cuenta la prevalencia de siete categorías de anomalías congénitas seleccionadas, se estimó el número de casos anuales esperados en base al total de nacimientos reportado en las estadísticas vitales. Según su presentación clínica, los casos con anomalías congénitas específicas fueron clasificados en: Casos aislados: presentan una anomalía congénita estructural mayor única, o dos o más anomalías congénitas mayores, solo si corresponden a una secuencia malformativa o se encuentran en la misma estructura corporal. Ejemplos: cardiopatía compleja, secuencia de espina bífida (con talipes equinovarus e hidrocefalia). Casos con AC múltiples: presentan dos o más anomalías congénitas estructurales mayores que afectan estructuras corporales diferentes no relacionadas, sin diagnóstico etiológico. Ejemplos: caso con fisura de labio y onfalocele, sin etiología definida. Síndromes: casos en los que la anomalía o anomalías estructurales mayores presentan una causa definida, sea genética o no. Ejemplos: síndrome de Down, embriopatía por zika10.
Resultados
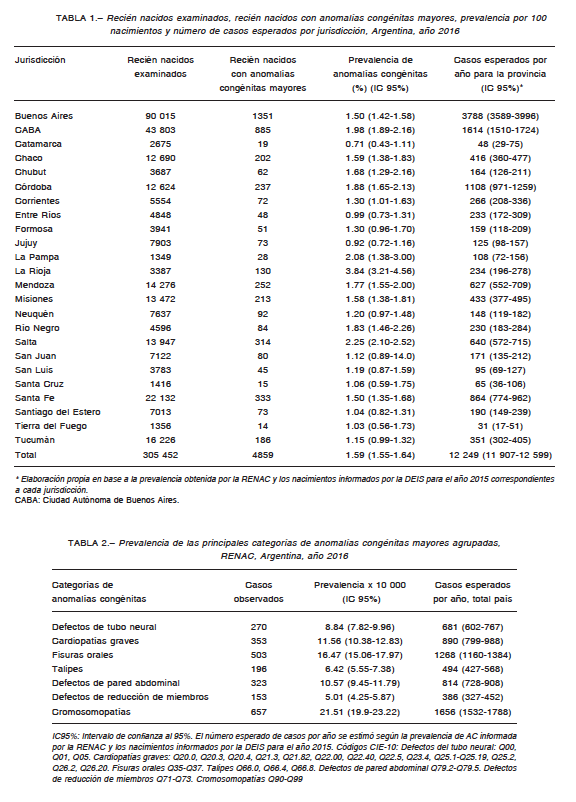
Del total de 305 452 nacimientos examinados en 2016, 4859 casos presentaron anomalías congénitas estructurales mayores, lo que representa una prevalencia al nacimiento de 1.59% (IC 95% 1.55-1.64) (Tabla 1).
Se detalla la prevalencia de 7 categorías de anomalías agrupadas: defectos del tubo neural, cardiopatías graves, fisuras orales, talipes, defectos de pared abdominal, defectos de reducción de miembros, cromosomopatías (Tabla 2).
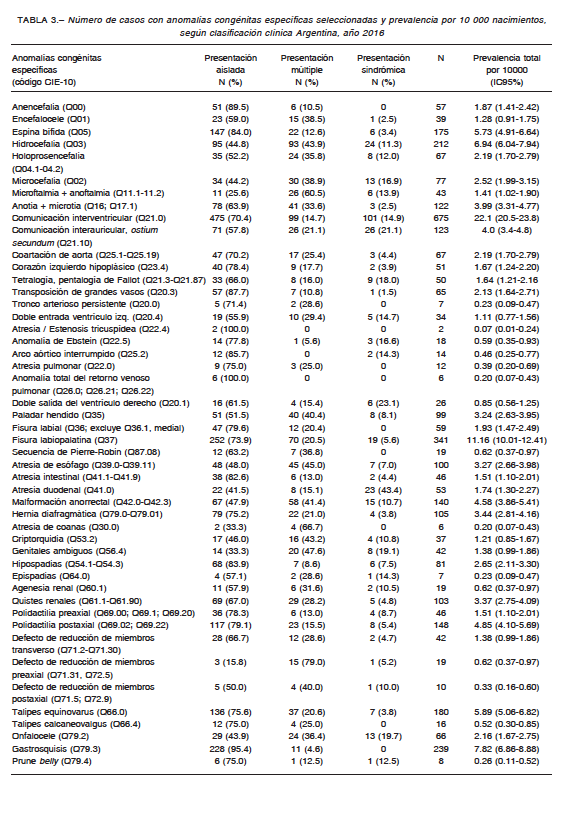
El número de casos y la prevalencia de 48 anomalías específicas seleccionadas de acuerdo a su frecuencia, importancia clínica y posibilidad de ser comparadas con otros registros del mundo se presentan en la Tabla 3. Las anomalías específicas más frecuentes fueron: las comunicaciones interventriculares, fisuras labiopalatinas (FLAP), gastrosquisis, hidrocefalia, talipes equinovarus, espina bífida, polidactilia postaxial, malformación anorrectal, hernia diafragmática, comunicación interauricular tipo ostium secundum, quistes renales y atresia de esófago.
Con respecto a los 3 síndromes cromosómicos más frecuentes, se observaron 548 casos de síndrome de Down (trisomía 21) (17.94 por 10 000; IC 95%: 16.47-19.51), 52 casos de síndrome de Edwards (trisomía 18) (1.70 por 10 000; IC 95%:1.27-2.23) y 19 casos de síndrome de Patau (trisomía 13) (0.62 por 10 000; IC95%: 0.37-0.97). La prevalencia de síndrome de Down en mujeres de 35 años o más fue de 72 por 10 000 (IC 95%: 64-80); mientras que en mujeres menores de 35 años fue de 9.6 por 10 000 (IC 95%: 8,4-10,8). Con respecto a gastrosquisis, la prevalencia en mujeres de 35 años o más fue de 0.19 por 10 000 (IC 95% 0.06-0.44) y en menores de 35 años fue de 8.9 por 10 000 (IC 95%: 7.6-10,1). La prevalencia de gastrosquisis en mujeres menores de 25 años fue mayor aún, de 15.1 por 10 000 (IC 95%: 13.0-17.4).
Discusión
El porcentaje de recién nacidos y fetos muertos con anomalías congénitas estructurales mayores, detectadas hasta el alta de la maternidad, observado a partir de los datos de la RENAC se encuentra dentro de los valores informados en la literatura, entre 1 y 3%11, 12. Los casos esperados anualmente de anomalías congénitas totales ilustran la dimensión de este problema de salud, dado que cada caso implica un impacto en el recién nacido, su familia, el sistema de salud y la sociedad. La jurisdicción con más casos esperados fue la provincia de Buenos Aires, dado que en esta provincia ocurre la mayor proporción de los nacimientos de todo el país.
En líneas generales, la cobertura de la RENAC ha aumentado a lo largo de los años, aunque es heterogénea entre las provincias, variando entre el 27% y 100% en el subsector público. El número estimado esperado de recién nacidos con anomalías congénitas varía entre 31 casos anuales en Tierra del Fuego, y 3788 en la provincia de Buenos Aires. Además del número total, los casos estimados esperados por grupo de anomalías congénitas son un insumo de utilidad para la planificación de recursos específicos para la prevención, atención y el cuidado de los afectados. La estimación sirve a las redes intra-provinciales que se articulan para el cuidado de los afectados con otros programas sanitarios, como el Programa Nacional de Cardiopatías Congénitas, la Red de atención FLAP13 y el Paquete Perinatal de Alta Complejidad (PPAC) SUMAR-CUS (Cobertura Universal de Salud-SUMAR) , entre otros.
La clasificación de los casos según su presentación clínica (aislados, múltiples y síndromes) permite conocer la proporción de pacientes que requerirán la resolución de una única anomalía en el caso de los aislados; qué proporción de casos serán de resolución más compleja y tendrán peor pronóstico, por presentar anomalías congénitas múltiples o síndromes; y cuáles necesitarán una evaluación y asesoramiento por un especialista en genética por tratarse de síndromes que puedan implicar algún riesgo de recurrencia en la familia.
La comparación entre los casos observados en RENAC según categorías de presentación clínica y lo informado en la literatura, permite evaluar la precisión de las descripciones de los casos que se notifican. Por ejemplo, si al realizar la comparación con la literatura, se observara que los informes a RENAC presentan una proporción más alta de casos aislados de una anomalía, la razón podría ser una deficiencia en la evaluación de anomalías asociadas o síndromes. Asimismo, la comparación entre la prevalencia de anomalías congénitas observada en RENAC y la notificada previamente por otros sistemas, permite identificar sub-registro.
La prevalencia de fisuras orales observada fue similar a la informada en la literatura14. En el caso del subtipo de fisura de paladar, este defecto está más frecuentemente asociado a otras anomalías congénitas, como cardiopatías, hidrocefalia, anomalías urogenitales y polidactilia, o formando parte de síndromes (por ejemplo, síndrome de microdeleción 22q11.2 y síndrome de Stickler, entre otros), en comparación con la fisura de labio, con o sin fisura de paladar15. Esta situación se observó también para los casos notificados a RENAC. Según publicaciones previas, la prevalencia de fisura de labio y paladar es mayor que la prevalencia de fisura de paladar, y la de fisura de labio, menor a las dos anteriores16. Este orden de frecuencias se observó también en los resultados obtenidos por RENAC.
En cuanto a los defectos del tubo neural, la prevalencia es un dato útil para evaluar los resultados de la fortificación obligatoria con ácido fólico (FAF) de la harina de trigo (Ley 25.630)17. Distintos estudios demostraron una caída significativa en la prevalencia y mortalidad por defectos de tubo neural (DTN) pos-fortificación con ácido fólico (FAF) en Argentina18,19. La prevalencia de DTN fue similar a la informada en la literatura en países donde existe fortificación con ácido fólico. La prevalencia de espina bífida fue mayor a la de anencefalia, mientras que la prevalencia de encefalocele fue menor a la de estas últimas, de manera consistente con la literatura20. Sin embargo, la prevalencia de anencefalia, una anomalía congénita invariablemente letal, fue más baja que la notificada por otros sistemas de vigilancia, lo cual podría deberse a un subregistro de fetos muertos, o la no inclusión de terminaciones electivas de embarazos, ilegales en nuestro país. Por lo tanto, la prevalencia de DTN podría ser más alta que la informada por RENAC. Si ese fuera el caso, existiría la posibilidad de lograr un descenso aun mayor en la prevalencia de DTN a través del consumo peri-concepcional de ácido fólico. Es importante evaluar la FAF no solo a través de la prevalencia de defectos del tubo neural, sino también monitoreando los niveles de folatos séricos y en glóbulos rojos en una muestra representativa de la población.
En cuanto a la presentación clínica de los defectos del tubo neural, los resultados fueron consistentes con informes previos: encefalocele se presentó con otras anomalías asociadas en mayor proporción que la espina bífida. El encefalocele se suele asociar a fisura de labio con o sin paladar, cardiopatías congénitas y defectos génito-urinarios, entre otros. También se encuentra formando parte de numerosos síndromes, como el Síndrome de Meckel Gruber, la trisomía 13 y la trisomía 18.
Con respecto a los defectos de pared abdominal, el onfalocele se presentó más frecuentemente en casos múltiples y sindrómicos que en formas aisladas, resultado consistente con lo ya informado21. El onfalocele se suele asociar a cardiopatías congénitas, anomalías urogenitales, defectos del tubo neural y anomalías cerebrales. Se observa en síndromes como las trisomías 13, 18 y 21, y el síndrome de Beckwith-Wiedeman, entre otros22. La prevalencia de gastrosquisis fue mayor a la de onfalocele. En este punto cabe destacar que la prevalencia de gastrosquisis observada en Argentina fue mayor a la de los registros de países más desarrollados11. El factor de riesgo conocido más importante que ha sido informado para gastrosquisis es la edad materna joven23. Esta prevalencia más alta en Argentina puede deberse a una diferencia en la estructura de edad materna en nuestra población, o a otros factores de riesgo de menor contribución. En forma consistente con la literatura, en RENAC la prevalencia de gastrosquisis fue mayor en mujeres jóvenes. La prevalencia de onfalocele fue similar a la hallada en otros sistemas de vigilancia11, por lo cual se descartan errores diagnósticos con gastrosquisis que pudieran aumentar de manera espuria la prevalencia de esta última anomalía.
En cuanto a los defectos de reducción de miembros, de acuerdo al eje afectado, se clasifican en defectos transversos (intercalares o terminales) o longitudinales (preaxiales, mesoaxiales o postaxiales). Se observó mayor afección terminal que el resto de los tipos, resultado consistente con la literatura24.
Con respecto a las cardiopatías congénitas graves, la prevalencia fue menor a la informada por otros sistemas11. Es importante considerar que los sistemas de vigilancia que muestran valores de prevalencia más altas amplían el período de detección más allá del alta de la maternidad, corresponden a países que han implementado el tamizaje con oximetría de pulso en forma sistemática, o incluyen las terminaciones de embarazo electivas por anomalía fetal.
Con respecto al síndrome de Down, se observó el aumento de la prevalencia en función de la edad de la madre, lo cual es consistente con la literatura25.
En cuanto a las limitaciones del presente trabajo, las prevalencias fueron estimadas a partir de datos hospitalarios con una cobertura parcial de los nacimientos del país, con mayor representación de instituciones públicas, por lo cual algunos factores socioeconómicos o demográficos podrían modificar las prevalencias.
En concusión, la RENAC es un sistema de vigilancia de la salud pública de AC estructurales mayores que funciona en forma continua desde 2009, generando informes periódicos de frecuencias de AC. En este trabajo presentamos los resultados correspondientes al año 2016, donde observamos una alta consistencia con lo ya informado en la literatura.
Agradecimientos: Agradecemos a todos los miembros de la Red Nacional de Anomalías Congénitas (RENAC) de Argentina que hicieron posible este trabajo a través del envío mensual de los datos sobre casos afectados por anomalías congénitas y números de nacimientos en sus respectivos hospitales. El presente trabajo forma parte de las acciones de la RENAC, que pertenece al Centro Nacional de Genética Médica, ANLIS, Ministerio de Salud. Ha sido parcialmente financiado por la Agencia Nacional de Promoción Científica y Tecnológica a través del PICT 2374-2014, la Dirección Nacional de Investigación para la Salud del Ministerio de Salud, y UNICEF Argentina.
Conflicto de intereses: Ninguno que declarar
Bibliografía
1. Christianson A, Howson CP, Modell B. Global Report on Birth Defects. The hidden toll of dying and disabled children. White Plains, New York: March of Dimes Birth Defects Foundation, 2006, p 1-85.
2. Dirección de Estadísticas e Información de Salud (DEIS), Estadísticas Vitales, Información Básica Año 2015. DEIS: Programa Nacional de Estadísticas de Salud 2016. En: http://www.deis.msal.gov.ar/wp-content/uploads/2016/09/2016-Tabla1.html; consultado junio de 2018.
3. Czeizel AE. Birth defects are preventable. Int J Med Sci 2005; 2: 91-2.
4. Cochi SL, Edmonds LE, Dyer K, et al. Congenital rubella syndrome in the United States, 1970-1985. On the verge of elimination. Am J Epidemiol 1989; 129: 349-61.
5. OMS. 63° Asamblea Mundial de la Salud. Punto 11.7. Defectos congénitos: Informe de la secretaria. Ginebra, 2010. En: http://apps.who.int/gb/ebwha/pdf_files/WHA63/A63_10-sp.pdf; consultado junio de 2018.
6. Groisman B, Bidondo MP, Barbero P, Gili J, Liascovich R y Grupo de Trabajo RENAC. Registro Nacional de Anomalías Congénitas de Argentina. Arch Argent Pediatr 2013; 111: 484-94.
7. Aase JM. Dysmorphologic diagnosis for the pediatric practitioner. Pediatr Clin North Am 1992; 39:135-56.
8. The Royal College of Paediatrics and Child Health adaptation of the International Statistical Classification of Diseases and Health Related Problems, 10th revision. London: Royal College of Paediatrics and Child Health; 2001.
9. Mason CA, Kirby RS, Sever LE, Langlois PH. Prevalence is the preferred measure of frequency of birth defects. Birth Defects Res A Clin Mol Teratol 2005; 73: 690-2.
10. Rasmussen SA, Olney RS, Holmes LB, Lin AE, Keppler-Noreuil KM, Moore CA. National Birth Defects Prevention Study. Guidelines for case classification for the National Birth Defects Prevention Study. Birth Defects Res (Part A): Clin Mol Teratol 2003; 67: 193-201.
11. Annual report. International Clearing House of birth defect surveillance and research, 2014. En: http://www.icbdsr.org/wp-content/annual_report/Report2014.pdf; consultado junio de 2018.
12. Centers for Disease Control and Prevention (CDC). Update on overall prevalence of major birth defects–Atlanta, Georgia, 1978-2005. MMWR Morb Mortal Wkly Rep 2008; 57: 1-5.
13. Cassinelli A, Pauselli N, Piola A, et al. Red nacional para la atención de niños/as con fisuras orales: organización, funcionamiento y primeros resultados. Arch Argent Pediatr 2018; 116: e26-e33.
14. Robert E, Kallen B, Harris J. The epidemiology of orofacial clefts.1. Some general epidemiological characteristics. J Craniofac Genet Dev Biol 1996; 16: 234-41.
15. Mossey PA, Modell B. Epidemiology of oral clefts 2012: an international perspective. Front Oral Biol 2012; 16:1.
16. Mossey PA, Little J, Munger RG, Dixon MJ, Shaw WC. Cleft lip and palate. Lancet 2009; 374: 1773-85.
17. Ley Nacional 25.630 (2002) En: http://www.anmat.gov.ar/Legislacion/Alimentos/Ley_25630.pdf; consultado junio de 2018.
18. Bidondo MP, Liascovich R, Barbero P, Groisman B. Prevalencia de defectos del tubo neural y estimación de casos evitados posfortificación en Argentina. Arch Argent Pediatr 2015; 113: 498-501.
19. López-Camelo JS, Castilla EE, Orioli IM. Folic acid flour fortification: impact on the frequencies of 52 congenital anomaly types in three South American countries. Am J Med Genet A 2010; 152A: 2444-58.
20. Zaganjor I, Sekkarie A, Tsang BL, et al. Describing the prevalence of neural tube defects worldwide: A systematic literature review. PLoS One 2016; 11: e05586.
21. Stoll C, Alembik Y, Dott B, et al. Omphalocele and gastroschisis and associated malformations. Am J Med Genet (Part A): 2008; 146A: 1280-5.
22. Forrester MB, Merz RD. Structural birth defects associated with omphalocele and gastroschisis, Hawaii, 1986-2001. Congenit Anom (Kyoto) 2008; 48: 87-91.
23. Castilla EE, Mastroiacovo P, Orioli IM. Gastroschisis: international epidemiology and public health perspectives. Am J Med Genet C Semin Med Genet 2008; 148C: 162-79.
24. Bedard T, Lowry RB, Sibbald B, Crawford S, Kiefer GN. Congenital limb deficiencies and major associated anomalies in Alberta for the years 1980-2012. Am J Med Genet (Part A): 2018; 176: 19-28.
25. Hecht CA, Hook EB. Rates of Down syndrome at livebirth by one-year maternal age intervals in studies with apparent close to complete ascertainment in populations of European origin: a proposed revised rate schedule for use in genetic and prenatal screening. Am J Med Genet 1996; 62: 376-85.
